Video
Indlægsseddel
Indlægsseddel: Information til brugeren
Terrosa 20 mikrogram/80 mikroliter injektionsvæske, opløsning i fyldt pen
teriparatid
Læs denne indlægsseddel grundigt, inden du begynder at bruge dette lægemiddel, da den indeholder vigtige oplysninger.
- Gem indlægssedlen. Du kan få brug for at læse den igen.
- Spørg lægen eller apotekspersonalet, hvis der er mere, du vil vide.
- Lægen har ordineret dette lægemiddel til dig personligt. Lad derfor være med at give lægemidlet til andre. Det kan være skadeligt for andre, selvom de har de samme symptomer, som du har.
- Kontakt lægen eller apotekspersonalet, hvis du får bivirkninger, herunder bivirkninger, som ikke er nævnt i denne indlægsseddel. Se punkt 4.
Se den nyeste indlægsseddel på www.indlaegsseddel.dk.
Oversigt over indlægssedlen
- Virkning og anvendelse
- Det skal du vide, før du begynder at bruge Terrosa
- Sådan skal du bruge Terrosa
- Bivirkninger
- Opbevaring
- Pakningsstørrelser og yderligere oplysninger
1. Virkning og anvendelse
Terrosa indeholder det aktive stof teriparatid, som anvendes til at styrke knoglerne og mindske risikoen for knoglebrud ved at fremme knogledannelse.
Terrosa anvendes til behandling af knogleskørhed hos voksne. Knogleskørhed er en sygdom, der gør dine knogler tynde og skrøbelige. Sygdommen er især almindelig hos kvinder efter overgangsalderen, men den kan også forekomme hos mænd. Knogleskørhed er også almindeligt forekommende hos patienter, der får lægemidler, som kaldes binyrebarkhormoner.
2. Det skal du vide, før de begynder at bruge Terrosa
Brug ikke Terrosa
- hvis du er allergisk over for teriparatid eller et af de øvrige indholdsstoffer i dette lægemiddel (angivet i punkt 6).
- hvis du har forhøjede niveauer af calcium (kalk) i blodet (eksisterende hyperkalcæmi).
- hvis du har alvorlige nyreproblemer.
- hvis du har haft knoglecancer, eller hvis en anden cancer har spredt sig til knoglerne (metastaser).
- hvis du har andre knoglesygdomme. Fortæl det til lægen, hvis du har en knoglesygdom.
- hvis du har et uforklarligt højt niveau i blodet af et bestemt enzym (basisk fosfatase), hvilket betyder, at du kan have Pagets sygdom (en sygdom med unormale knogleforandringer). Spørg din læge, hvis der er noget, du er i tvivl om.
- hvis du har fået strålebehandling, som påvirker dine knogler.
- hvis du er gravid eller ammer.
Advarsler og forsigtighedsregler
Terrosa kan øge calcium (kalk) i blodet eller urinen.
Kontakt lægen, før eller mens du tager Terrosa:
- Hvis du lider af vedvarende kvalme, opkastning, forstoppelse, nedsat energi eller muskelsvaghed. Dette kan være tegn på, der er for meget calcium (kalk) i dit blod.
- Hvis du lider af nyresten eller har haft nyresten.
- Hvis du har nyreproblemer (moderat nedsat nyrefunktion).
Nogle patienter oplever svimmelhed eller hjertebanken efter de første indsprøjtninger med Terrosa. Når du tager de første doser af Terrosa, så gør det et sted, hvor du har mulighed for at sidde eller ligge ned, hvis du skulle blive svimmel.
Den anbefalede behandlingstid på 24 måneder bør ikke overskrides.
Inden du tager en ny fyldt pen i brug, skal du skrive lægemidlets batchnummer (lot-nummer) og den første injektionsdato ned på den fyldte pens ydre karton og i en kalender, og angive denne information ved rapportering af eventuelle bivirkninger.
Terrosa må ikke bruges af patienter, der stadig vokser.
Børn og unge
Terrosa må ikke bruges til børn og unge (under 18 år).
Brug af andre lægemidler sammen med Terrosa
Fortæl det altid til lægen eller apotekspersonalet, hvis du bruger andre lægemidler, for nylig har brugt andre lægemidler eller planlægger at brug andre lægemidler.
Det er vigtigt, da nogle lægemidler (f.eks. digoxin/digitalis, et lægemiddel til behandling af hjertesygdomme) kan påvirke teriparatid.
Graviditet og amning
Du må ikke anvende Terrosa, hvis du er gravid eller ammer. Hvis du er kvinde i den fødedygtige alder, skal du anvende sikre præventionsmetoder, når de bruger Terrosa. Hvis du bliver gravid, mens du bruger Terrosa, skal behandlingen med Terrosa ophøre. Spørg din læge eller apotekspersonalet til råds, inden du tager dette lægemiddel.
Trafik- og arbejdssikkerhed
Nogle patienter kan føle sig svimle efter en indsprøjtning med Terrosa. Hvis du føler dig svimmel, må du ikke køre bil eller betjene værktøj eller maskiner, før du har det bedre.
Terrosa indeholder natrium
Dette lægemiddel indeholder mindre end 1 mmol (23 mg) natrium pr. dosis, dvs. det er i det væsentlige ”natriumfrit”.
3. Sådan skal du bruge Terrosa
Brug altid lægemidlet nøjagtigt efter lægens anvisning. Er du i tvivl, så spørg lægen eller apotekspersonalet.
Den anbefalede dosis er 20 mikrogram (svarende til 80 mikroliter) én gang om dagen, som gives som indsprøjtning under huden (subkutan injektion) i låret eller maven.
Som en hjælp til at huske at tage lægemidlet, bør du tage indsprøjtningen på omtrent samme tidspunkt hver dag. Terrosa kan indsprøjtes i forbindelse med måltider.
Du skal tage Terrosa hver dag i så lang tid, som din læge har udskrevet det til dig. Den totale behandlingstid med Terrosa bør ikke overskride 24 måneder. Du bør ikke få mere end én behandlingskur på 24 måneder i din levetid.
Din læge vil muligvis anbefale, at du anvender Terrosa sammen med calcium (kalk) og D-vitamin. Din læge vil fortælle dig, hvor meget du skal tage hver dag.
Terrosa kan gives med eller uden mad.
De kompatible kanyler følger ikke med Terrosa.
Pennen kan bruges med kanyler udviklet i overensstemmelse med ISO-standarden for penkanyler, der måler mellem 29 G og 31 G (diameter: 0,25 – 0,33 mm) og har en længde på mellem 5 mm og 12,7 mm, udelukkende til subkutan injektion.
For korrekt brug af dette lægemiddel er det meget vigtigt, at du nøje følger den brugsanvisning, der følger med den fyldte pen.
Brug en ny kanyle til hver injektion for at forhindre kontaminering, og bortskaf kanylen på sikker vis efter brug.
Opbevar aldrig pennen med påsat kanyle.
Overfør ikke lægemidlet til en injektionssprøjte.
Du skal indsprøjte Terrosa umiddelbart efter, at du har taget pennen ud af køleskabet. Sæt hætten på pennen, og læg straks pennen tilbage i køleskabet efter brug. Opbevar den i køleskabet før og under hele behandlingsperioden på 28 dage.
Klargøring til injektion
- Læs altid brugsanvisningen til Terrosa fyldt pen, som følger med i lægemiddelæsken, for at sikre korrekt administration af Terrosa.
- Vask hænderne inden håndtering af pennen.
- Tjek udløbsdatoen på etiketten på den fyldte pen, inden du begynder at bruge lægemidlet. Sørg for, at der er mindst 28 dage tilbage inden udløbsdatoen. Skriv batchnummeret (lot-nummeret) og den første injektionsdato for den pågældende pen ned. Datoen for den første injektion skal desuden skrives på Terrosas ydre karton (se det dertil beregnede felt på kartonen: {Første anvendelse:}).
- Sæt en ny kanyle på den fyldte pen, og indstil dosen i displayvinduet ved at dreje på doseringsknappen.
Injektion af Terrosa
- Inden injektion af Terrosa, skal huden renses på det tilsigtede injektionssted (låret eller maven) som anvist af lægen.
- Tag forsigtigt fat i en ren hudfold, og indfør kanylen lige ind i huden. Tryk på doseringsknappen, og hold den nede i mindst seks sekunder for at sørge for, at du har modtaget hele dosen.
- Så snart injektionen er færdig, skal du sætte den ydre beskyttelseshætte på penkanylen og skrue hætten mod uret for at fjerne penkanylen. Derved forbliver den resterende Terrosa steril, og lækage fra pennen forebygges. Det forhindrer desuden luft i at komme ind i pennen såvel som tilstopning af kanylen.
- Sæt hætten på pennen igen.
- Bortskaf penkanylerne på sikker vis i en kanylebeholder eller i henhold til lægens anvisninger.
Hvis du har brugt for meget Terrosa
Hvis du ved en fejltagelse har taget mere Terrosa, end du skulle, skal du kontakte din læge eller apoteket. De forventede virkninger af en overdosis omfatter kvalme, opkastning, svimmelhed og hovedpine.
Hvis du har glemt at bruge Terrosa
Hvis du glemmer en injektion eller ikke kan tage lægemidlet på det sædvanlige tidspunkt, skal du tage den snarest muligt samme dag. Du må ikke tage en dobbeltdosis som erstatning for den glemte dosis. Tag ikke mere end én indsprøjtning samme dag.
Hvis du holder op med at bruge Terrosa
Hvis du overvejer at holde op med at bruge Terrosa, skal du tale med din læge om det først. Din læge kan råde dig og beslutte, hvor længe du skal behandles med Terrosa.
Spørg lægen eller apotekspersonalet, hvis der er noget, du er i tvivl om.
4. Bivirkninger
Dette lægemiddel kan som alle andre lægemidler give bivirkninger, men ikke alle får bivirkninger.
De mest almindelige bivirkninger er smerter i arme og ben (frekvensen er meget almindelig; kan forekomme hos flere end 1 ud af 10 patienter). Andre almindelige bivirkninger (kan forekomme hos op til 1 ud af 10 patienter) inkluderer kvalme, hovedpine og svimmelhed. Hvis du bliver svimmel efter indsprøjtningen, skal du sætte eller lægge dig ned, indtil du får det bedre. Hvis du ikke får det bedre, skal du kontakte lægen, før du fortsætter med behandlingen. Der er set tilfælde af besvimelse efter teriparatid-behandling.
Hvis du oplever ubehag rundt om injektionsstedet, såsom rødmen i huden, smerter, hævelser, kløe, blå mærker eller mindre blødninger (som kan forekomme almindeligt), skal dette aftage i løbet af få dage eller uger. I modsat fald skal du fortælle det til din læge.
I sjældne tilfælde (kan forekomme hos op til 1 ud af 1 000 patienter) oplever nogle patienter allergiske reaktioner i form af vejrtrækningsbesvær, hævelse af ansigtet, udslæt og brystsmerter. Disse reaktioner forekommer som regel lige efter injektion. Der kan i sjældne tilfælde opstå alvorlige og potentielt livstruende allergiske reaktioner, herunder anafylaksi.
Andre bivirkninger omfatter:
Almindelige (kan forekomme hos op til 1 ud af 10 patienter)
- forhøjelse af blodets kolesterolniveau
- depression
- nervesmerter i benene
- mathedsfornemmelse
- fornemmelse af, at alting drejer rundt
- uregelmæssig puls
- åndenød
- øget svedtendens
- muskelkramper
- nedsat energi
- træthed
- brystsmerter
- lavt blodtryk
- halsbrand (smertefuld og brændende følelse bag brystbenet)
- opkastning
- en udposning på spiserøret (hernia hiatus esophagi)
- lavt hæmoglobin eller lavt antal af røde blodlegemer (blodmangel, anæmi)
Ikke almindelige (kan forekomme hos op til 1 ud af 100 patienter):
- øget hjertefrekvens (puls)
- unormal hjertelyd
- stakåndethed
- hæmorroider
- urininkontinens
- øget vandladningstrang
- vægtforøgelse
- nyresten
- smerter i muskler og led. Nogle patienter har haft alvorlige rygkramper eller smerter, der medførte indlæggelse.
- stigning i blodets calciumindhold
- stigning i blodets indhold af urinsyre
- stigning i et enzym ved navn basisk fosfatase
Sjældne (kan forekomme hos op til 1 ud af 1 000 patienter):
- nedsat nyrefunktion, inklusive nyresvigt
- hævelser, hovedsagelig af hænder, fødder og ben
Indberetning af bivirkninger
Hvis du oplever bivirkninger, bør du tale med din læge eller apotekspersonalet. Dette gælder også mulige bivirkninger, som ikke er medtaget i denne indlægsseddel. Du eller dine pårørende kan også indberette bivirkninger direkte til Lægemiddelstyrelsen via det nationale rapporteringssystem anført i Appendiks V. Ved at indrapportere bivirkninger kan du hjælpe med at fremskaffe mere information om sikkerheden af dette lægemiddel.
5. Opbevaring
Opbevar lægemidlet utilgængeligt for børn.
Brug ikke lægemidlet efter den udløbsdato, der står på kartonen og den fyldte pen efter EXP. Udløbsdatoen er den sidste dag i den nævnte måned.
Skal altid opbevares i køleskab (2 °C-8 °C). Pennen skal lægges tilbage i køleskabet umiddelbart efter brug. Må ikke nedfryses.
Lad hætten være på pennen for at beskytte den mod lys.
Du kan anvende Terrosa i op til 28 dage efter den første indsprøjtning, så længe pennen opbevares i et køleskab (2 °C til 8 °C).
For at undgå nedfrysning må pennen ikke lægges tæt på en eventuel frostboks i køleskabet. Terrosa må ikke bruges, hvis det er eller har været nedfrosset.
Hver pen skal bortskaffes på forsvarlig vis 28 dage efter første brug, også selvom den ikke er fuldstændig tom.
Terrosa indeholder en klar og farveløs opløsning. Terrosa må ikke anvendes, hvis opløsningen er uklar, farvet eller indeholder partikler.
Spørg apotekspersonalet, hvordan du skal bortskaffe lægemiddelrester. Af hensyn til miljøet må du ikke smide lægemiddelrester i afløbet, toilettet eller skraldespanden.
6. Pakningsstørrelser og yderligere oplysninger
Terrosa indeholder:
- Aktivt stof: teriparatid. Hver dosis på 80 mikroliter indeholder 20 mikrogram teriparatid. En fyldt pen med 2,4 ml indeholder 600 mikrogram teriparatid (svarende til 250 mikrogram per ml).
- Øvrige indholdsstoffer: iseddikesyre; koncentreret, mannitol, metacresol, natriumacetattrihydrat, saltsyre (til pH-justering), natriumhydroxid (til pH-justering), vand til injektionsvæsker (se punkt 2 ”Terrosa indeholder natrium”).
Udseende og pakningsstørrelser
Terrosa er en farveløs og klar injektionsvæske, opløsning (injektion). Det fås i en fyldt pen. Hver fyldt pen indeholder 2,4 ml opløsning, svarende til 28 doser.
Pakningsstørrelser: 1 fyldt pen eller 3 fyldte penne i en karton.
Ikke alle pakningsstørrelser er nødvendigvis markedsført.
Indehaver af markedsføringstilladelsen og fremstiller
Gedeon Richter Plc.
Gyömrői út 19-21.
1103 Budapest
Ungarn
Denne indlægsseddel blev senest ændret
Andre informationskilder Detaljeret information om produktet kan også fås ved at scanne QR-koden angivet nedenfor eller på yderpakningen med en smartphone. De samme oplysninger kan desuden findes på den følgende URL: www.terrosapatient.com

Du kan finde yderligere oplysninger om dette lægemiddel på Det Europæiske Lægemiddelagenturs hjemmeside: http://www.ema.europa.eu
Brugsanvisning
Terrosa 20 mikrogram (µg)/80 mikroliter injektionsvæske, opløsning i fyldt pen
Brugsanvisning
Vigtige oplysninger
Den fyldte Terrosa Pen er til administration af en daglig fast dosis på 80 mikroliter Terrosa injektionsvæske, opløsning til behandling af osteoporose.
Deres fyldte pen indeholder 28 doser.
Det er ikke muligt at indstille en dosis til andet end 80 mikroliter.
Hvis du ikke kan indstille dosen på 80 mikroliter, er din pen næsten tom.
Terrosa Pen kan ikke fyldes igen og må ikke anvendes efter 28 doser.
Oversigt over dele
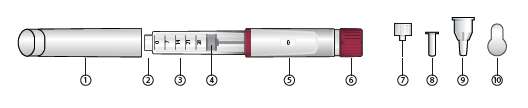
1. Hætte
2. Kanylegevind
3. Cylinderampulholder
4. Cylinderampulstempel
5. Displayvindue
6. Doseringsknap
7. Penkanyle
8. Indre kanylebeskyttelse
9. Ydre kanylehætte
10. Aftagelig forsegling
Penkanylen medfølger ikke i pakningen med pennen. Den skal sættes på inden brug af pennen (se trin 1c).
Før du starter
Læs hele brugsanvisningen, før du begynder at bruge din nye Terrosa Pen. Følg anvisningerne nøje, når du bruger pennen. Læs også den medfølgende indlægsseddel.
Notér datoen for din første injektion i en kalender.
Del ikke din pen eller dine kanyler med andre, da det indebærer en risiko for overførsel af smitstoffer.
Vask hænder før hver injektion.
Brug ikke din Terrosa Pen, hvis den er beskadiget, eller hvis du er i tvivl om, hvorvidt den fungerer korrekt.
Klargør alt, hvad du har brug for:
• spritservietter
• den fyldte pen
• en penkanyle
1. Klargør din pen
1/a Tag hætten af pennen
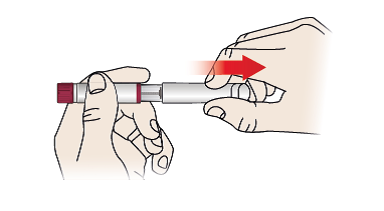
- Træk hætten (1) af pennen
1/b Kontrollér lægemidlet
- Tjek etiketten på Terrosa Pen for at være sikker på, at du får det rigtige lægemiddel, og at det ikke er udløbet.
- Brug ikke din Terrosa Pen, hvis:
- pennen er beskadiget.
- opløsningen er uklar, farvet eller indeholder partikler.
1/c Sæt kanylen på
- Brug en ny penkanyle til hver injektion, og brug kun de anbefalede penkanyler, der fremgår af afsnittet ”Kompatible penkanyler” på bagsiden af denne brugsanvisning.
- Brug ikke penkanylen, hvis den aftagelige forsegling er beskadiget eller løs – bortskaf den, og brug en anden.
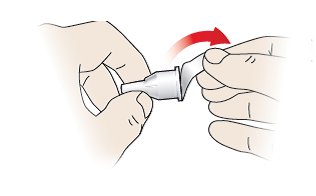
- Fjern den aftagelige forsegling (10).
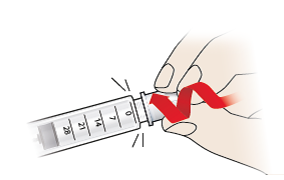
- Tryk kanylen på spidsen af pennen, og skru den godt fast.
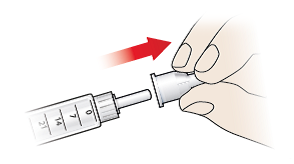
- Træk den ydre kanylehætte (9) af, og gem den, da du skal bruge den til at fjerne kanylen med senere. Lad den indre kanylebeskyttelse (8) sidde på kanylen for at undgå stikskader.
2. Injektion
2/a Indstil dosis
Din pen indeholder 28 faste doser à 80 mikroliter. Denne faste dosis skal indstilles ved hver daglige injektion.
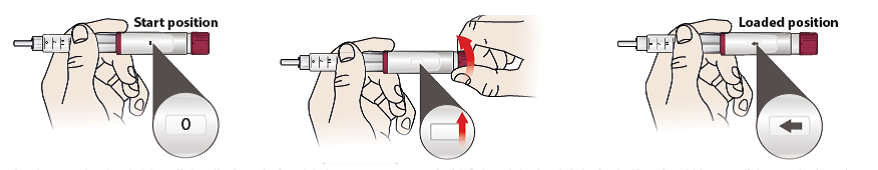
- Drej på doseringsknappen (6), indtil displayvinduet (5) viser et pilesymbol, og knappen bliver låst – Du kan høre et klik, når dosen bliver indstillet korrekt.
- Pilesymbolet betyder, at den faste daglige dosis er indstillet, og at pennen er klar til injektion.
- Hvis du ikke kan indstille dosen, er pennen næsten tom. Brug en anden pen.
2/b Vælg injektionssted
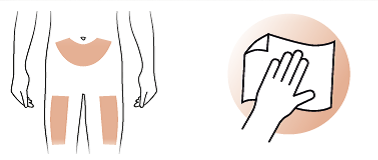
- Injektionen skal gives i maven eller øverste del af låret. Klargør huden i henhold til lægens anbefalinger.
- Rengør det valgte område med en spritserviet.
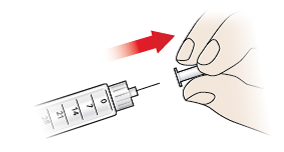
- Træk forsigtigt den indre kanylebeskyttelse (8) af, og bortskaf den med det samme.
2/c Indgiv dosen
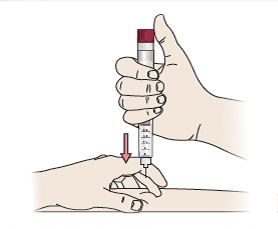
- Hold forsigtigt om en hudfold med tommel- og pegefinger. Indfør forsigtigt kanylen i huden i en ret vinkel.
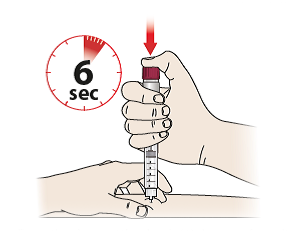
- Tryk doseringsknappen (6) så langt ned, som den kan komme, og hold den nede i mindst 6 sekunder, så du er sikker på, at hele dosen bliver indgivet – du hører et klik, når du begynder at trykke på knappen, hvilket er normalt.
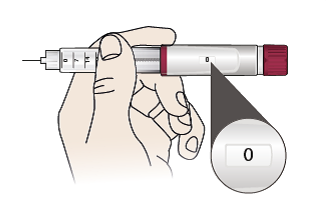
- Træk pennen langsomt ud. Vigtigt: Kontrollér, at displayet viser ’0’.
3. Efter injektionen
3/a Fjern kanylen
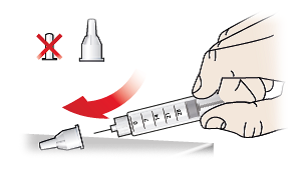
- Skub forsigtigt den ydre kanylehætte (9) tilbage på penkanylen (7).
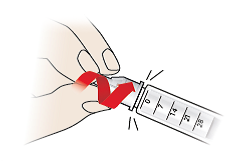
- Tag fat om den ydre kanylehætte (9), og skru penkanylen af (7).
- Bortskaf altid penkanylerne på sikker vis i en kanylebeholder eller i henhold til lægens anvisninger.
3/b Opbevaring af din pen
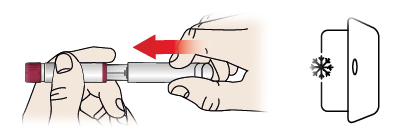
- Sæt hætten (1) på pennen igen.
- Læg pennen tilbage i køleskabet mellem 2 og 8 °C umiddelbart efter brug.
3/c Bortskaffelse af pennen

Når du skal bortskaffe pennen efter 28 dages brug, skal du gøre det forsigtigt, og som beskrevet i afsnittet “Bortskaffelse af Terrosa Pen og brugte kanyler” på bagsiden af denne brugsanvisning.

Fejlfinding
Følg instruktionerne i tabellen, hvis du har spørgsmål angående brugen af Terrosa Pen:
| Problem | Løsning |
| 1. Der ses små luftbobler i cylinderampullen. | En lille luftboble vil ikke påvirke dosen eller medføre skade. |
| 2. Kanylen kan ikke sættes fast. | Brug en anden kanyle i stedet. Kontakt kundeservice, hvis den anden kanyle heller ikke kan sættes fast. |
| 3. Kanylen er ødelagt/bøjet/knækket. | Brug en anden kanyle i stedet. |
| 4. Jeg forsøgte ved et uheld at foretage injektionen uden en påsat kanyle. | Sæt en kanyle på. Du vil se nogle dråber komme ud. Pennen er nu klar til brug igen. Indstil dosen, og gennemfør injektionen. |
| 5. Doseringsknappen kan ikke drejes op til pilesymbolet. | Mængden af lægemiddel, der er tilbage i Terrosa Pen, er mindre end 80 mikroliter. Brug en ny Terrosa Pen. |
| 6. Displayet vender ikke tilbage til positionen ’0’ efter injektionen. | Gentag ikke injektionen på den samme dag. Brug en ny kanyle, og gennemfør injektionen den næste dag. Brug ikke denne pen, hvis displayet stadig ikke vender tilbage til positionen ’0’ efter injektionen. Kontakt kundeservice. |
| 7. Der observeres spild fra pennen. | Brug ikke denne pen. Kontakt kundeservice. |
Andre vigtige oplysninger
- Den fyldte Terrosa Pen indeholder 28 daglige faste doser à 80 mikroliter Terrosa injektionsvæske, opløsning til behandling af osteoporose.
- Overfør ikke lægemidlet til en injektionssprøjte.
- Brug kun din Terrosa Pen, som anvist af din læge, i denne brugsanvisning og i indlægssedlen til Terrosa.
- Brug en ny kanyle til hver injektion.
- Terrosa Pen kan bruges af patienter over 18 år, der injicerer sig selv, af sundhedspersoner og af tredjeparter såsom voksne familiemedlemmer.
- Terrosa Pen må ikke bruges af blinde eller synshæmmede patienter uden hjælp fra en oplært og rask person. Kontakt din læge i tilfælde af høre- eller håndteringsproblemer.
Kontakt vores kundeservice, hvis du har spørgsmål vedrørende brug af Terrosa Pen.
Telefonnummer: XXXXXXXXXX
E-mail: XXXXXXXX
Kompatible penkanyler
- Clickfine penkanyle 29 til 31 gauge (diameter 0,25-0,33 mm) og en længde på 12, 10, 8 eller 6 mm.
- BD Micro-Fine penkanyle 29 til 31 gauge (diameter 0,25-0,33 mm) og en længde på 12,7, 8 eller 5 mm.
Opbevaring og vedligeholdelse af Terrosa Pen
- Opbevar ikke Terrosa Pen med en isat kanyle, da dette kan medføre, at der dannes luftbobler i cylinderampullen.
- Transportér og opbevar Terrosa Pen ved temperaturer mellem 2-8 °C.
- Opbevar ikke din Terrosa Pen i fryseren. Bortskaf pennen, og brug en ny Terrosa Pen, hvis lægemidlet har været nedfrosset.
- Opbevar din Terrosa Pen og penkanylerne utilgængeligt for børn.
- Håndter din pen forsigtigt. Undgå at tabe pennen og at lade den ramme ind i hårde overflader. Beskyt den mod vand, støv og fugt.
- En fugtig klud er nok til at rengøre Terrosa Pen. Brug ikke alkohol, andre opløsningsmidler eller rengøringsmidler. Nedsænk aldrig Terrosa Pen i vand, da dette kan beskadige den.
- Brug ikke din Terrosa Pen, hvis den er beskadiget, eller hvis du er i tvivl om, hvorvidt den fungerer korrekt.
Bortskaffelse af Terrosa Pen og brugte kanyler
- Terrosa Pen skal bortskaffes 28 dage efter første brug.
- Før du bortskaffer Terrosa Pen, skal du altid fjerne penkanylen.
- Læg brugte kanyler i en kanylebeholder eller anden beholder af hård plast med et sikret låg. Du må ikke smide kanylerne direkte i skraldespanden.
- Du må ikke genbruge den fyldte kanylebeholder.
- Spørg lægen eller apotekspersonalet, hvordan du skal bortskaffe pennen og kanylebeholderen.
- Anvisningerne vedrørende kanylehåndtering er ikke ment som en erstatning for lokale, sundhedsprofessionelle eller institutionelle politikker.
Indehaver af markedsføringstilladelsen: Gedeon Richter Plc., Ungarn
Fremstillet af Gedeon Richter Plc., Ungarn
Denne brugermanual blev senest ændret


